В осадочной оболочке земной коры сосредоточены огромные залежи природного газа. Согласно теории биогенного (органического) происхождения нефти, они образуются в результате разложения останков живых организмов. Считается, что природный газ образуется в осадочной оболочке при больших температурах и давлениях, чем нефть. С этим согласуется тот факт, что месторождения газа часто расположены глубже, чем месторождения нефти.
Огромными запасами природного газа обладают Россия (Уренгойское месторождение), Иран, большинство стран Персидского залива, США <#»513373.files/image001.gif»>
где М i — молекулярная масса i-го компонента;
x i — объемное содержание i-го компонента, доли ед.
Для реальных газов обычно М=16 — 20.
Плотность газа ρ г рассчитывается по формуле:
![]() ,
,
где V м — объем 1 моля газа при стандартных условиях.
Обычно ρ г находится в пределах 0,73 — 1,0 кг/м3 .
Плотность газа в значительной степени зависит от давления и температуры, и поэтому для практического применения этот показатель неудобен. Чаще пользуются относительной плотностью газа по воздуху ρ г.в. , равной отношению плотности газа ρг к плотности воздуха ρв , взятой при тех же давлении и температуре:
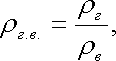
Если ρ г и ρв определяются при стандартных условиях, то ρв = 1,293 кг/м3 и ρг.в. = ρг / 1,293.
Плотность нефтяных газов колеблется от 0,554 (для метана) до 2,006 (для бутана) и выше.
Вязкость газа характеризует силы взаимодействия между молекулами газа, которые преодолеваются при его движении. Она увеличивается при повышении температуры, давления и содержания углеводородных компонентов. Однако при давлениях выше 3МПа увеличение температуры вызывает понижение вязкости газа.
Вязкость нефтяного газа незначительна и при 0 о С составляет 0,000131 пз; вязкость воздуха при 0о С равна 0,000172 пз.
Уравнения состояния газов используются для определения многих физических свойств природных газов. Уравнением состояния называется аналитическая зависимость между параметрами газа, описывающая поведение газа. Такими параметрами являются давление, объем и температура.
Происхождение нефти и газа (3)
... давления, температуры и растворенного в нефти газа. Зависимость вязкости от давления весьма незначительная; с увеличением температуры вязкость нефти уменьшается; с увеличением количества растворенного газа она заметно уменьшается. Вязкость нефти ... разведочных работ в СССР и в США завершилось открытием залежей, связанных с соляными куполами, приподнимающими, а иногда и протыкающими осадочные толщи. ...
Состояние идеальных газов в условиях высоких давления и температуры определяется уравнением Клапейрона — Менделеева:
![]() ,
,
где р — давление;
V и — объем идеального газа;число киломолей газа;
- R- универсальная газовая постоянная;
- Т — температура.
Идеальным называется газ, силами взаимодействия между молекулами которого пренебрегают. Реальные углеводородные газы не подчиняются законам идеальных газов. Поэтому уравнение Клапейрона-Менделеева для реальных газов записывается в виде:
![]()
где Z — коэффициент сверхсжимаемости реальных газов, зависящий от давления, температуры и состава газа и характеризующий степень отклонения реального газа от закона для идеальных газов.
Коэффициент сверхсжимаемости Z реальных газов — это отношение объемов равного числа молей реального V и идеального V и газов при одинаковых термобарических условиях (т. е. при одинаковых давлении и температуре):
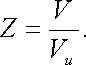
Значения коэффициентов сверхсжимаемости наиболее надежно могут быть определены на основе лабораторных исследований пластовых проб газов. При отсутствии таких исследований (как это чаще всего бывает на практике) прибегают к расчетному методу оценки Z по графику Г. Брауна (рисунок 1).
Для пользования графиком необходимо знать, так называемые, приведенные псевдокритическое давление и псевдокритическую температуру. Критической называется такая температура, выше которой газ не может быть превращен в жидкость ни при каком давлении. Критическим давлением называется давление, соответствующее критической точке перехода газа в жидкое состояние.
С приближением значений давления и температуры к критическим свойства газовой и жидкой фаз становятся одинаковыми, поверхность раздела между ними исчезает и плотности их уравниваются.
С появлением в системе двух и более компонентов в закономерностях фазовых изменений возникают особенности, отличающие их поведение от поведения однокомпонентного газа. Не останавливаясь на подробностях, следует отметить, что критическая температура смеси находится между критическими температурами компонентов, а критическое давление смеси всегда выше, чем критическое давление любого компонента.
Для определения коэффициента сверхсжимаемости Z реальных газов, представляющих собой многокомпонентную смесь, находят средние из значений критических давлений и температур каждого компонента. Эти средние называются псевдокритическим давлением p п.кр. и псевдокритической температурой Тп.кр. Они определяются из соотношений:
Состав и физические свойства природного газа
... состояния газов используются для определения многих физических свойств природных газов. Уравнением состояния называется аналитическая зависимость между параметрами газа, описывающая поведение газа. Такими параметрами являются давление, объем и температура. Состояние идеальных газов в ...
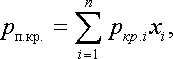
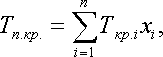
где р кр. и Ткр. — критические давления и температура i-го компонента;
x i — доля i-го компонента в объеме смеси (в долях единицы).
Приведенные псевдокритические давление и температура, необходимые для пользования графиком Брауна, представляют собой псевдокритические значения, приведенные к конкретным давлению и температуре (к пластовым, стандартным или каким-либо другим условиям):
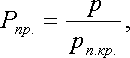
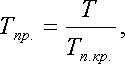
где р и Т — конкретные давления и температура, для которых определяется Z.
Коэффициент сверхсжимаемости Z обязательно используется при подсчете запасов газа для правильного определения изменения объема газа при переходе от пластовых условий к поверхностным, при прогнозировании изменения давления в газовой залежи и при решении других задач.
Вопрос классификации природных газов очень сложен, так как они имеют разнообразный состав, различное происхождение, разные условия нахождения и физическое состояние в природе. Кроме того, газы обладают большой эмиграционной способностью, создают различные смеси и редко бывают однородными по химическому составу. Одновременно с процессами образования газов идут процессы их разрушения. Например, при действии кислорода на сероводород образуется свободная сера и вода.
Первую классификацию природных газов составил В.И. Вернадский (1912), где он указал, что при изучении газов необходимо знать три следующие фактора: форму или условия нахождения газов в природе, источники их происхождения или генезис и химический состав. Согласно этим факторам В.И. Вернадский выделил три группы газов.
I. По форме нахождения:
А. Свободные газы: 1) атмосферные, 2) газовые скопления, содержащиеся в порах горных пород и окклюзии, 3) газовые струи или вихри (вулканические, тектонические, поверхностные), 4) газовые испарения.
Б. Жидкие растворы газов: 1) газы океанов и морей, 2) газы озер, прудов и рек, 3) газы различных водных источников (вулканических, тектонических, поверхностных).
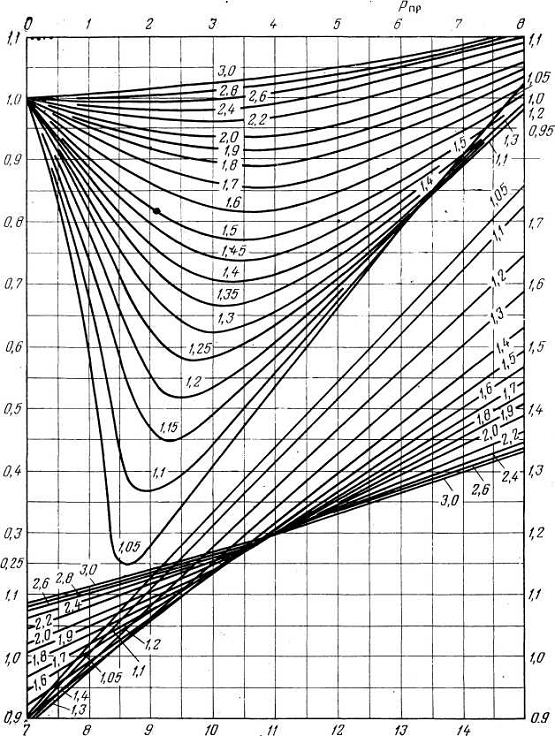
Рисунок 1 — Графики зависимости коэффициента сверхсжимаемости Z углеводородного газа от приведенных псевдокритических давления рпр. и температуры Тпр. (по Г.Брауну).
В. Твердые растворы газов (газы адсорбированные горными породами и минералами).. По источникам происхождения: 1) газы земной поверхности, 2) газы, связанные с высокотемпературными очагами литосферы, 3) газы глубинные, проникающие в земную кору из мантии.. По составу (разделение для тектонических газов): 1) азотные, 2) углекислые, 3) метановые, 4) водородные, 5) сероводородные, 6) водяные пары.
Особенности разработки газовых месторождений. Классификация месторождений ...
... кольцевых или линейных цепочек скважин. газовый месторождение скважина 3. Технологический режим эксплуатации газовых скважин В процессе добычи газа из газовой залежи скважины, шлейфы, сепараторы, теплообменники, абсорберы, ... химическому составу выделил три основных типа газов: 1) углеводородные, 2) углекислые и 3) азотные. Генетическое направление в классификации В.И. Верданского в дальнейшем было ...
Позже, в развитие этой классификации был создан целый ряд классификационных схем природных газов по условиям нахождения и физическому состоянию в природе, по химическому составу, генезису и по их практической ценности и содержанию полезных компонентов. В отечественной литературе опубликовано более 20 классификаций природных газов только по химическому составу.
Ряд классификационных схем разработали М.И. Суббота и А.Ф. Романюк, которые приведены ниже.
3.1 Классификация по условиям нахождения газа в природе. Газы земной поверхности:
- тропосферы;
- стратосферы и мезосферы;
- атмосферных осадков;
- пещер и карстовых полостей.. Газы поверхностной гидросферы:
- океанов и морей;
- рек, озер и прудов;
- поверхностных льдов;
- болот.. Газы, рассеянные в горных породах:
- в порах и трещинах осадочных пород;
- сорбированные породами;
- поровых растворов;
- магматогенных пород;
- газово-жидкие включения в минералах;
- илов;
- газогидратов илов;
- почв.. Газы подземной гидросферы:
- грунтовых вод;
- вод зоны свободного водообмена;
- вод зоны затрудненного водообмена;
- мерзлых вод и газогидратов.. Свободные газы залежей:
- газовых залежей;
- газовых шапок нефтяных залежей;
- газоконденсатных залежей;. Газы, растворенные и сорбированные в биогенных ископаемых:
- растворенные в нефти;
- сорбированные углями;
- в горючих сланцах.. Газы грязевых вулканов:
- грязевых извержений;
- грязевых грифонов.. Газы магматических очагов и поствулканических процессов:
- вулканических извержений;
- фумарольные;
- пневматогенных внедрений;
- гидротермальных растворов.. Газы живых организмов:
- животных;
- высших растений;
- микроорганизмов.
3.2 Классификация по генезису газов. Газы биохимического генезиса:
микробиологического преобразования ОВ илов и почв — СО 2 , СН4 , N2 , CO, N2 O, NO2 , H2 , NH3 , H2 S и др.;
микробиологического преобразования торфа — СО 2 , N2 , СН4 , CO, H2 S, NH3 и др.;
микробиологического преобразования углей — СО 2 , СН4 , N2 , CO, H2 и др.;
микробиологического преобразования нефти — СН 4 , СО2 и др.;
Фотосинтеза зеленых растений — О 2 ;
жизнедеятельности высших растений — СО 2 , CO, С2 Н4 , летучих ОВ и др.;
жизнедеятельности животных — СО 2 , CO, H2 S, СН4 , летучих ОВ и др.;
микробиологического разложения растений и животных — СО 2 , CO, СН4 , H2 S, N2 , NH3 и др.. Газы химического генезиса:
химического генезиса в нормальных условиях земной поверхности — СО 2 и др.;
термических реакций — СН 4 , CO, СО2 и др. (150-300 о С);
термокаталитических реакций — СН 4 , Cn H2n , H2 , CO и др.. Газы дегазации мантии:
дегазации мантии — СН 4 , H2 , NH3 , N2 , СО2 , SO2 , H2 S, СО, H2 O и др.;
остаточные первичной атмосферы Земли — Ar, N 2 и др.. Газы радиоактивного распада и радиохимического генезиса, генерирующиеся на участках распространения радиоактивных элементов — Не, Ar, Rn, H2 , O2 и др.. Газы, образующиеся под воздействием космических лучей, генерирующиеся в верхних слоях атмосферы: атомарные — Н, Не и др.; изотопы — Н2 , О2 , N2 , О3 , NО и другие.
3.3 Классификация газов по химическому составу. Преимущественно метановый (СН 4 > 50 %):
метановый (СН 4 > 75 %);
метано-азотный (СН 4 > 50 %);
метан-этан-пропановый (СН 4 > 50 %);
метано-углекислый (СН 4 > 50 %).. Преимущественно углеводородный (тяжелее метана, ТУ >50 %):
- этан-пропановый (ТУ >
- 75 %);
- этан-пропан-метановый (ТУ >
- 50 %).. Преимущественно азотный (N 2 >
- 50 %):
азотный (N 2 > 75 %);
азотно-метановый (N 2 > 50 %);
азотно-углекислый (N 2 >50 %);
азотно-кислородно-углекислый (N 2 > 50 %).. Преимущественно углекислый (СО2 > 50 %):
углекислый (СО 2 > 75 %);
углекисло-азотный (СО 2 > 50 %);
углекисло-метановый (СО 2 > 50 %);
углекисло-сероводородный (СО 2 > 50 %).. Преимущественно водородный (Н2 > 50 %):
водородный (Н 2 > 75 %);
водородно-азотный (Н 2 > 50 %).
1.3.4 Классификация газов по их практической ценности. Горючие газы (энергетическое и химическое сырье):
- чисто метановых залежей;
- метановых, обогащенных тяжелыми углеводородами;
- газоконденсатных залежей;
- нефтяных месторождений;
- метановых и угольных месторождений;
- метановых водорастворимых.. Газы, обогащенные инертными компонентами:
- гелий в углеводородных газовых залежах и водах;
- гелий в азотных залежах;
- азотных залежей.. Газы, обогащенные сероводородом:
- сероводород в метановых залежах;
- сероводород в углеводородных газовых залежах..
Углекислые газы минеральных вод.
3.5 Классификация и индексация В.И. Старосельского, классификация В.А. Соколова
Существует классификация и индексация природных газов по содержанию полезных компонентов В.И. Старосельского, которая основана на требованиях промышленности по минимальной концентрации компонентов, являющихся ценным химическим сырьем. Среди неуглеводородных компонентов газа в ней учитывается азот (А), углекислый газ (У), сероводород (Св), а среди углеводородных компонентов — метан (Н), этан (Э), тяжелые углеводороды (Т) и конденсат (К).
В зависимости от пределов процентного содержания какого-либо компонента в газе, около его буквенного индекса ставится цифра от 1 до 4. Состав газа обозначается суммой индексов. Например, состав газов Астраханского газоконденсатного месторождения будет выражен следующим индексом: М 2 Э1 Т2 У4 А1 Св4 К4 . Он означает, что газ содержит метана от 30 до 70 %, этана менее 3 %, тяжелых углеводородов 5-10 %, углекислого газа более 15 %, азота менее 3 %, сероводорода более 1 % и конденсата более 200 г/м3 .
Природные газы подразделяются в этой классификации по содержанию этана, который является ценным химическим сырьем, а также — по содержанию тяжелых УВ на метановые, этановые, этан-пропановые и пропан-бутановые. Метановые газы характерны для газовых скоплений. Они содержат метана от 90 до100 %, этана до 3 % и тяжелых УВ до 5 %. Этановые газы содержат этана от 3 до 6 % , тяжелых УВ от 5 до 10 %, а этан-пропановые газы — этана от 6 до 9 %, тяжелых УВ — от 10 до 30 %. Эти газы характерны, в основном, для газоконденсатных и нефтегазоконденсатных залежей. В пропан-бутановых газах концентрация тяжелых УВ составляет более 30 % и этана более 9 %. Они характерны для нефтяных залежей.
Широко известна классификация природных газов по условиям нахождения, химическому составу и генезису, составленная В.А. Соколовым (таблица 5).
Таблица 5 — Классификация природных газов по В.А. Соколову (1966)
|
Тип газа по условиям нахождения в природе |
Химический состав |
Происхождение газа |
|
|
Основные компоненты |
Важнейшие примеси |
||
|
1 |
2 |
3 |
4 |
|
I. Газы атмосферные |
N 2 , O2 |
Ar, CO 2 , Ne, He, Kr, Xe, H2 , O3 |
Смесь газов химического, биохимического и радиогенного происхождения (Не, Ar) |
|
II. Газы земной поверхности: |
|||
|
1) почвенные и подпочвенные |
CO 2 , N2 , O2 |
Ar, CH 4 , N2 O, H2 , благородные газы (из атмосферы) |
CO 2 , CH4 , N2 O, H2 преимущественно биохимического происхождения, присутствует также воздух |
|
2) болотные и торфяные |
СН 4 , CO2 , N2 |
Ar, H 2 , CO, NH3 , N2 O, H2 S, благородные газы (из атмосферы) |
СН 4 , CO2 , H2 , NH3 , N2 O, H2 S преимущественно биохимического происхождения |
|
3) морских субаквальных осадков |
CO 2 , CH4 , N2 |
H 2 , NH3 , H2 S, Ar |
Все газы, кроме благородных, преимущественно биохимического происхождения |
|
III. Газы осадочной толщи: |
Все газы, кроме благородных, главным образом химического происхождения. Имеется примесь газов биохимического происхождения (частично H 2 S и др.). На значительных глубинах при повышенной температуре нормальная |
||
|
1) нефтяных месторождений |
CH 4 , ТУВ, N2 , CO2 |
H 2 S, He, Ar, H2 |
|
|
2) газовых месторождений |
CH 4 , C2 H6 , N2 , CO2 |
ТУВ, H 2 S, He, Ar, H2 |
|
|
3) угольных месторождений |
СН 4 |
CO 2 , N2 , H2 , ТУВ, H2 S, NH3 , He, Ar |
|
|
4) соленосных отложений |
N 2 , H2 , CO2 , CH4 |
H 2 S, ТУВ, N2 , H2 |
деятельность микроорганизмов прекращается и биохимические газы там отсутствуют |
|
5) пластовых вод |
N 2 , H2 , CO2 |
O 2 , ТУВ, H2 S, H2 , Ar |
|
|
IV. Газы океанов и морей |
CO 2 , N2 |
NH 3 , H2 S, О2 и частично СО2 биохимического происхождения, часть СО2 и N2 образуется химическим путём, а Ar имеет радиогенное происхождение. В верхние слои океанов и морей СО2 , N2 и О2 попадают из атмосферы |
|
|
V. Газы метаморфических пород |
N 2 , H2 , CO2 |
СН 4 , H2 S, He, Ar |
Газы, кроме благородных химического происхождения |
|
VI. Газы магматических пород |
H 2 , CO2 |
N 2 , H2 S, He, Ar. На больших глубинах SO2 , HCl, HF |
Газы, кроме благородных химического происхождения |
|
VII. Газы вулканические |
Все газы, кроме благородных химического происхождения. Они представляют собой в той или иной степени изменённые газы, поступающие из верхней мантии с примесью газов из вышерасположенных оболочек |
||
|
1) высокотемпературные (из лавовых озёр и др.) |
H 2 , CO2 , SO2 , HCl, HF |
N 2 , CO, NH3 , He, Ar |
|
|
2) фумарольные (100-300 0 С) |
H 2 , CO2 , SO2 , H2 S |
N 2 , CO, NH3 , He, Ar |
|
|
3) термальных источников [Электронный ресурс]//URL: https://drprom.ru/kursovaya/prirodnyiy-gaz/ |
CO 2 |
N 2 , CO, NH3 , He, Ar |
|
|
VIII. Газы космоса |
Н 2 , Н, Не |
СО, радикалы СН, СН 2 , ОН и другие. Ионизированные атомы элементов Ne, N, Ar |
Все газы являются результатом ядерных, радиационно-химических и химических реакций |
2. Методы определения состава природных газов
Компонентный состав газов определяется хроматографическим <#»513373.files/image012.gif»>
Рисунок 2 — Хроматограф Varian 3800
Для анализа используется трехканальная хроматографическая система Varian 3800 модель С (анализатор природного газа, рисунок2), позволяющая анализировать углеводородный состав газа, неуглеводородный состав газа, а также водород. Анализатор поставляется после тестирования на заводе Varian с предустановленной программой анализа.
Водород и гелий определяются методом газоадсорбционной хроматографии с детектором по теплопроводности (рисунок 3).
Неуглеводородные (и углеводородные) компоненты определяются методом газоадсорбционной хроматографии с детектором по теплопроводности (рисунок 4) (а также углеводородные).
Анализ углеводородных компонентов осуществляется методом капиллярной газожидкостной хроматографии с пламенно-ионизационным детектором (рисунок 5).
Рисунок 3 — Газоадсорбционная хроматография
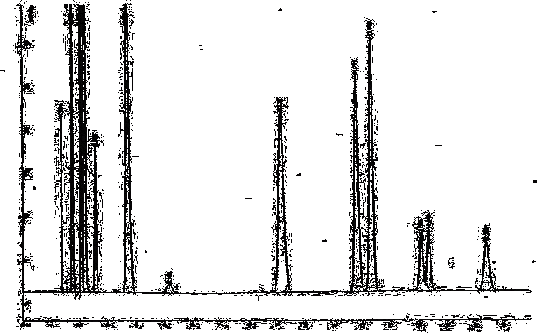
Рисунок 4 — Газоадсорбционная хроматография (1 — кислород/аргон, 2 — азот, 3 — метан, 4 — диоксид углерода, 5 — этан, 6 — сероводород, 7 — пропан, 8 — изобутан, 9 — бутан, 10 — изопентан, 11 — н-пентан, 12 — гексаны)
2.3 Газожидкостная хроматография
(а. gas-liquid chromatography; н. Gas- Flьssigkeits-Chromatographie; ф. Chroma- tographie gaz-liquide; и. cromatografнa lнquido-gas) — метод разделения и анализа смесей газо- или парообразных веществ, основанный на их различной растворимости в тонком слое жидкости, нанесённой на твёрдый носитель.
Метод газожидкостной хроматографии предложен английский учёными А. Джеймсом и А. Мартином в 1952. В процессе разделения компоненты смеси распределяются между неподвижной жидкой и подвижной газовой (газ-носитель) фазами. Коэффициент распределения — отношение концентраций компонента в двух фазах — для различных
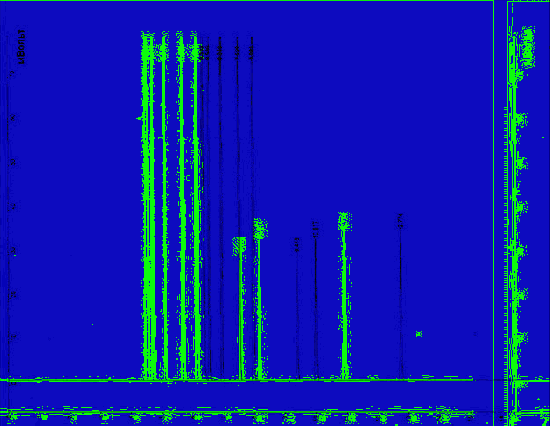
Рисунок 5 — Метод капиллярной газожидкостной хроматографии
(1 — метан, 2 — этан, 3 — пропан, 4 — изобутан, 5 — бутан, 6 — изопентан, 7 — пентан, 8 — гексаны) веществ различны. По механизму разделения газожидкостная хроматография относится к распределительной хроматографии. По форме проведения процесса газожидкостной хроматографии подразделяют на колоночную и капиллярную. В колоночной газожидкостной хроматографии слой нелетучей в условиях эксперимента жидкости (трикрезилфосфат, сорбитол, полиэтиленгликоль и др.) наносят на поверхность зёрен носителя (хромосорб, тефлон, кизельгур и др.), которым затем наполняют колонку. В капиллярной газожидкостной хроматографии жидкую фазу наносят непосредственно на стенки капилляров. Для анализа сложных смесей наиболее широкое распространение получили элюентный и вытеснительный способы. Чувствительность газожидкостной хроматографии зависит от используемой аппаратуры, условий проведения анализа и составляет обычно 10-4-10-8%. Относительная ошибка определений колеблется от 2 до 5%.
Газожидкостную хроматографию широко применяют для анализа газов, жидкостей и твёрдых веществ. При анализе нелетучих веществ определяемые компоненты предварительно с помощью химических реакций переводят в летучие соединения (т.н. реакционная хроматография).
Например, Cu, Cr, Mn, Fe, Co, Ni в горных породах <http://www.mining-enc.ru/g/gornye-porody/> определяют в виде их хелатов; S, Se, Te, As и Bi в природных и сточных водах <http://www.mining-enc.ru/s/stochnye-vody/>
- после переведения их соединений в летучие гидриды.
Заключение
Природный газ — смесь газов <http://ru.wikipedia.org/wiki/%D0%93%D0%B0%D0%B7>, образовавшаяся в недрах земли при анаэробном разложении <http://ru.wikipedia.org/wiki/%D0%90%D0%BD%D0%B0%D1%8D%D1%80%D0%BE%D0%B1%D0%BD%D0%BE%D0%B5_%D1%80%D0%B0%D0%B7%D0%BB%D0%BE%D0%B6%D0%B5%D0%BD%D0%B8%D0%B5> органических веществ <http://ru.wikipedia.org/wiki/%D0%9E%D1%80%D0%B3%D0%B0%D0%BD%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B8%D0%B5_%D0%B2%D0%B5%D1%89%D0%B5%D1%81%D1%82%D0%B2%D0%B0>.
Природный газ относится к полезным ископаемым <http://ru.wikipedia.org/wiki/%D0%9F%D0%BE%D0%BB%D0%B5%D0%B7%D0%BD%D1%8B%D0%B5_%D0%B8%D1%81%D0%BA%D0%BE%D0%BF%D0%B0%D0%B5%D0%BC%D1%8B%D0%B5>. Природный газ в пластовых условиях (условиях залегания в земных недрах) находится в газообразном состоянии — в виде отдельных скоплений (газовые залежи) или в виде газовой шапки нефтегазовых месторождений, либо в растворённом состоянии в нефти или воде. При нормальных условиях (101,325 кПа <http://ru.wikipedia.org/wiki/%D0%9F%D0%B0%D1%81%D0%BA%D0%B0%D0%BB%D1%8C_(%D0%B5%D0%B4%D0%B8%D0%BD%D0%B8%D1%86%D0%B0_%D0%B8%D0%B7%D0%BC%D0%B5%D1%80%D0%B5%D0%BD%D0%B8%D1%8F)> и 20 °С) природный газ находится только в газообразном состоянии. Так же природный газ может находиться в виде естественных газогидратов <http://ru.wikipedia.org/wiki/%D0%93%D0%B0%D0%B7%D0%BE%D0%B2%D1%8B%D0%B5_%D0%B3%D0%B8%D0%B4%D1%80%D0%B0%D1%82%D1%8B>.
Природные газовые гидраты представляют собой метастабильный минерал, образование и разложение которого зависит от температуры, давления, химического состава газа и воды, свойств пористой среды <http://ru.wikipedia.org/w/index.php?title=%D0%9F%D0%BE%D1%80%D0%B8%D1%81%D1%82%D0%B0%D1%8F_%D1%81%D1%80%D0%B5%D0%B4%D0%B0&action=edit&redlink=1> и др.
В последние годы (после проведения в 2003 году совещания <http://gazprom.ru/press/news/2003/april/article54324/|газогидратного> в ОАО «Газпром» <http://ru.wikipedia.org/wiki/%D0%9E%D0%90%D0%9E_%C2%AB%D0%93%D0%B0%D0%B7%D0%BF%D1%80%D0%BE%D0%BC%C2%BB>
- исследования гидратов в России продолжались в различных организациях как посредством госбюджетного финансирования (два интеграционных проекта Сибирского отделения РАН <http://ru.wikipedia.org/wiki/%D0%A0%D0%90%D0%9D>, небольшие гранты РФФИ, грант губернатора Тюмени, грант министерства высшего образования РФ), так и за счет грантов международных фондов — ИНТАС, СРДФ, ЮНЕСКО (по программе «плавучий университет» — морские экспедиции под эгидой ЮНЕСКО под лозунгом Training Through Research — обучение через исследования), КОМЕКС (Kurele-Okhosk-Marine Experiment), ЧАОС (Carbon-Hydrate Accumulations in the Okhotsk Sea) и др.
В 2002 — 2004 гг. исследования по нетрадиционным источникам углеводородов, включая газовые гидраты (с учетом коммерческих интересов ОАО «Газпром» <http://ru.wikipedia.org/wiki/%D0%9E%D0%90%D0%9E_%C2%AB%D0%93%D0%B0%D0%B7%D0%BF%D1%80%D0%BE%D0%BC%C2%BB>
- , продолжались в ООО «Газпром ВНИИГАЗ» <http://ru.wikipedia.org/wiki/%D0%92%D0%9D%D0%98%D0%98%D0%93%D0%90%D0%97>
- и ОАО «Промгаз» <http://ru.wikipedia.org/wiki/%D0%9F%D1%80%D0%BE%D0%BC%D0%B3%D0%B0%D0%B7>
- при небольшом масштабе финансирования. В настоящее время исследования по газовым гидратам проводятся в ОАО «Газпром» <http://ru.wikipedia.org/wiki/%D0%9E%D0%90%D0%9E_%C2%AB%D0%93%D0%B0%D0%B7%D0%BF%D1%80%D0%BE%D0%BC%C2%BB>
- (главным образом, в ООО «Газпром ВНИИГАЗ» <http://ru.wikipedia.org/wiki/%D0%9E%D0%9E%D0%9E_%C2%AB%D0%93%D0%B0%D0%B7%D0%BF%D1%80%D0%BE%D0%BC_%D0%92%D0%9D%D0%98%D0%98%D0%93%D0%90%D0%97%C2%BB>
- , в институтах Российской академии наук, в университетах.
Природный газ широко применяется в качестве горючего в жилых частных и многоквартирных домах для отопления, подогрева воды и приготовления пищи; как топливо <http://ru.wikipedia.org/wiki/%D0%A2%D0%BE%D0%BF%D0%BB%D0%B8%D0%B2%D0%BE> для машин <http://ru.wikipedia.org/wiki/%D0%90%D0%B2%D1%82%D0%BE%D0%BC%D0%BE%D0%B1%D0%B8%D0%BB%D1%8C>, котельных <http://ru.wikipedia.org/wiki/%D0%9A%D0%BE%D1%82%D0%B5%D0%BB%D1%8C%D0%BD%D0%B0%D1%8F>, ТЭЦ <http://ru.wikipedia.org/wiki/%D0%A2%D0%AD%D0%A6> и др. Сейчас он используется в химической промышленности как исходное сырьё для получения различных органических веществ, например пластмасс. В XIX веке <http://ru.wikipedia.org/wiki/XIX_%D0%B2%D0%B5%D0%BA> природный газ использовался в первых светофорах <http://ru.wikipedia.org/wiki/%D0%A1%D0%B2%D0%B5%D1%82%D0%BE%D1%84%D0%BE%D1%80> и для освещения (применялись газовые лампы <http://ru.wikipedia.org/w/index.php?title=%D0%93%D0%B0%D0%B7%D0%BE%D0%B2%D1%8B%D0%B5_%D0%BB%D0%B0%D0%BC%D0%BF%D1%8B&action=edit&redlink=1>).
В экологическом отношении природный газ является самым чистым видом минерального топлива. При сгорании его образуется значительно меньшее количество вредных веществ по сравнению с другими видами топлива. Однако сжигание человечеством огромного количества различных видов топлива, в том числе природного газа, за последние полвека привело к некоторому незначительному увеличению содержания углекислого газа в атмосфере, который является парниковым газом. Некоторые ученые на этом основании делают вывод об опасности возникновения парникового эффекта и как следствие — резкого потепления климата. В связи с этим в 1997 г. некоторыми странами был подписан Киотский протокол по ограничению парникового эффекта. По состоянию на 26 марта 2009 Протокол был ратифицирован 181 страной мира (на эти страны совокупно приходится более чем 61 % общемировых выбросов).
Протокол является первым успешным рыночным механизмом по уменьшению выбросов парниковых газов в атмосферу. Следующим шагом было внедрение в действие с весны 2004 года негласной альтернативной глобальной программы ускоренного преодоления последствий техноэкологического кризиса. Основой программы стало установление адекватного ценообразования на энергоносители по их топливной калорийности. Цена определяется исходя из стоимости получаемых энергий на конечном потреблении из единицы измерения энергоносителя. С августа 2004 года по август 2007 года было рекомендовано и поддерживалось регуляторами соотношение $0,10 за киловатт-час (средняя стоимость нефти $68 за баррель).
С августа 2007 года была произведена ревальвация соотношения до $0,15 за киловатт-час (средняя стоимость нефти $102 за баррель).
Финансово-экономический кризис внёс свои коррективы, но указанное соотношение будет восстановлено регуляторами. Отсутствие управляемости на рынке газа задерживает установление адекватного ценообразования. Средняя стоимость газа при указанном соотношении $648 за 1000 н. метров кубических.
Библиография
[Электронный ресурс]//URL: https://drprom.ru/kursovaya/prirodnyiy-gaz/
1. Российская газовая энциклопедия. Москва. Научное издательство «Большая Российская энциклопедия», 2004, с.81-85.
- Мирзаджанзаде А.Х., Аметов И.М., Ковалев А.Г. Физика нефтяного и газового пласта. Изд. «Недра». М. 1982г — 268.
- Истомин В.А., Якушев В.С., Махонина Н.А., Квон В.Г., Чувилин Е.М.
Эффект самоконсервации газовых гидратов — Газовая промышленность, спецвыпуск «Газовые гидраты», 2006, с. 36-46.
4. История нефти в осадочных бассейнах: сб. науч. тр. / Под ред. Б.А. Соколова. — М.: Изд-во «Интерпринт», 1994 — 181.
- Карцев А.А. Основы геохимии нефти и газа. — М.: Недра, 1978 — 461.
- Новые идеи в геологии и геохимии нефти и газа.
Нефтегазовая геология — итоги ХХ века. — М.: Изд-во Моск. ун-та, 2000 — 386.
