Сырьём для получения свинца служат сульфидные и окисленные руды. В сульфидных рудах свинец в основном находится в виде минерала PbS, который называется свинцовым блеском или галенитом. В окисленных никелевых рудах свинец содержится виде минералов: церуссита PbCO 3 и англезита PbSO4 . Основное количество свинца получают из сульфидных руд. Находящиеся в природе свинцовые руды, как правило, являются комплексными. Основными спутниками свинца в рудах являются: цинк, медь и серебро. Содержание цинка в рудах зачастую превышает содержание свинца. Свинцово-цинковые руды представляют собой главную сырьевую базу свинца.
В сульфидных рудах цинк содержится в виде минерала сфалерита ZnS, который часто называют цинковой обманкой. Железо содержится в виде пирита FeS 2 и пирротина Fe7 S8 . Серебро содержится в виде минерала аргентита AgS. В окисленных рудах цинк содержится в виде смитсонита ZnCO3 , а серебро — в виде металла или AgCl.
Медь содержится в сульфидных рудах в виде халькопирита CuFeS 2 и ковеллина СuS, а в окисленных рудах в виде малахита CuCO3 ·Cu (OH) 2 и азурита Cu3 CO3 (OH) 2 .
В полиметаллических рудах обычно встречаются также золото, висмут, сурьма, мышьяк, кадмий, олово, галлий, таллий, индий, германий, селен, теллур.
Пустая порода представлена кварцем, баритом, кальцитом, и небольшими количествами силикатов алюминия, железа, магния и кальция.
Примерный состав свинцово-цинковых руд колеблется в следующих пределах по основным компонентам (%): Pb-1,2-2,3; Zn-1,35-4,0; Cu-0,5-1,0; Fe-1,8-8,5; S-5,0-16,0.
Из-за незначительного содержания ценных металлов свинцово-цинковые руды подвергаются процессу обогащения, которое осуществляется обычно флотацией, В результате обогащения свинцово-цинковых руд получают свинцовый, медный, цинковый и пирротиновый концентраты. В процессе обогащения благородные металлы распределяются в основном между медным и свинцовым концентратами. Незначительная часть золота попадает в пирротиновый концентрат.
Свинцовые концентраты, получаемые из свинцовых руд, имеют следующий состав (%): Pb-39-78; Zn-2-15; Cu-2-7; Fe-14-20.
В настоящее время значительное количество свинца получают из вторичного сырья, которое представляет собой отходы свинца и различные свинцовые сплавы.
Свинец и его свойства
... в разных образцах свинцовых руд может несколько различаться, что не дает возможности определить для свинца значение Arс большей точностью. В земной коре свинца немного - 0,0016% по массе, но этот ... путем заливки отверстий легкоплавким свинцом. Позднее при раскопках Микен нашли свинцовые скобы в каменных стенах. При получении свинца античные металлурги сначала прокаливали руду, при этом шли реакции ...
Среди различных способов, применяемых для получения свинца, наибольшее распространение получила шахтная плавка. Перед шахтной плавкой свинцовый концентрат подвергается обжигу и спеканию. Обжиг и спекание осуществляется на агломерационных машинах ленточного типа. Цель обжига и спекания — превращение сульфидов в оксиды и получение агломерата. Загружаемая на агломерационную ленту сульфидная шихта в голове машины зажигается с помощью горна, в котором сжигают углеводородное топливо. На поверхности шихты сульфиды воспламеняются в потоке горячих топочных газов горна. Далее по мере движения ленты горящий слой перемещается сверху вниз за счет просасывания через слой шихты воздуха, кислород которого окисляет сульфиды. Реакции окисления сульфидов протекают с большим выделением тепла. Температура в горящем слое поддерживается в пределах 1000-1100 о C. В горящем слое происходит разложение высших сульфидов FeS2 , CuFeS2 , CuS и протекают следующие основные реакции окисления низших сульфидов:
2PbS + 3O 2 = 2PbO + 2SO2
ZnS + 3O 2 = 2ZnO + 2SO2
Сu 2 S + 3O2 = 2Cu2 O + 2SO2
2FeS + 5O 2 = 2Fe2 O3 +2SO2
Сульфиды сурьмы и мышьяка также превращаются в оксиды.
При избытке кислорода сернистый газ окисляется до SO 3 , который реагирует с оксидами и образует сульфаты:
PbO + SO 3 = PbSO4 + SO3 = ZnSO42 O + 2SO3 + 0,5O2 = 2CuSO4
Оксиды свинца и кадмия, сульфиды свинца, сурьмы и олова при температурах обжига имеют заметные давления паров и поэтому частично удаляются с отходящими газами.
В процессе обжига кислотные оксиды реагируют с основными оксидами и образуют силикаты, ферриты, арсенаты и антимонаты свинца, железа, цинка и других металлов. В результате образуются легкоплавкие соединения, эвтектики и сплавы, которые при температуре обжига расплавляются и при охлаждении цементируют шихту, образуя твёрдый прочный и пористый агломерат.
Шихта для выплавки чернового свинца в шахтной печи (рисунок 1)
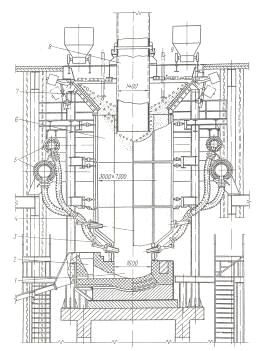
- горн;
- 2 — сифон для выпуска свинца;
- 3 — нижний ряд фурм;
- 4-верхний ряд фурм;
- 5 — коллекторы дутья;
- 6 — шахта печи;
- 7 — колошник;
- 8-газоход;
- 9 — уровнемерстолба шихты.
Рисунок 1 Устройство шахтной печи свинцовой плавки состоит из агломерата или спечённых окатышей, флюсов и кокса.
В качестве флюса обычно используется золото содержащий кварц. Крупность основной массы до 100 мм. Содержание мелкой фракции до 20 мм не должно превышать 10-15%. Шихта загружается сверху через колошниковое устройство, снизу через фурмы подаётся воздушное дутьё или дутьё, обогащённое кислородом.
По изменениям, которые происходят в шихте в процессе плавки шахтную печь можно разбить на пять зон.
Первую зону условно называют зоной подогрева. Температура в ней составляет до 400 о С. В этой зоне шихта подсушивается поступающими снизу печными газами и отдаёт им гигроскопическую и частично химически связанную влагу. Здесь начинаются также процессы восстановления свободных оксидов свинца и меди:
Реферат металлургия свинца
... По указанным причинам современная металлургия свинца практически полностью базируется на использовании технологических схем, включающих восстановительную плавку. Прямое восстановление сульфидов традиционными углеродистыми восстановителями ... 2 или 4. Температура плавления свинца 327,4°С, температура кипения 1740°С. Плотность твердого свинца 11,35 г/см3, с повышением температуры после перехода металла ...
PbO + CO = Pb + CO 22 O + CO = 2Cu + CO2
Вторую зону можно назвать верхней зоной восстановления. В ней поддерживается температура 400-700 о С. здесь шихта полностью теряет гидратную влагу и начинается разложение карбонатов и некоторых сульфидов. В этой зоне продолжается восстановление свободных оксидов и начинается восстановление различных сульфидов:
PbSO 4 + 4CO = PbS + CO24 + CO = ZnS + CO2
В этой зоне в достаточном количестве накапливается восстановленный свинец. Он в виде в виде крупных капель протекает между кусками шихты. В процессе омывания кусков шихты расплавленным свинцом, в него извлекаются благородные металлы и металлическая медь.
Третью зону называют зоной нижнего восстановления. В ней поддерживается температура 700-900 о С. Здесь практически заканчиваются реакции, протекающие во второй зоне. Здесь интенсивно разлагаются карбонаты кальция, магния и происходит сульфидирование свободных металлов и некоторых оксидов парами элементарной серы по реакциям:
2SO 2 + 4CO = S2 +4CO2
Pb + S 2 = 2PbS, 2Cd + S2 = 2CdS
Cu + S 2 = 2Cu2 S
Кроме того, в этой зоне протекают реакции образования летучих соединений мышьяка As 2 O3 и сурьмы Sb2 O3 и их нелетучих соединений As3 O5 и Sb3 O5 .
В третьей зоне интенсивно протекает реакция окисления углерода кокса углекислым газом:
CO 2 + C = 2CO.
В этой зоне образуется достаточное количество штейна, капли которого способны течь между кусками шихты.
Четвёртая зона представляет собой зону плавления. Здесь поддерживается температура порядка 1250 — 1300 о С той зоне происходит основной процесс горения углерода кокса:
С + О 2 = СО2
Здесь заканчиваются все выше описанные реакции и интенсивно протекают реакции штейно — и шлакообразования:
FeO + SiO 2 = 2FeO·SiO2 + SiO2 = CaO·SiO2
(Cu 2 O) + [FeS] = [Cu2 S] + (FeO)
[Cu] + [PbS] = [Cu 2 S] + [Pb]
Все составляющие шихты в этой зоне переходят либо в расплав, либо в газовую фазу.
Пятая зона представляет собой горн. Температура в горне составляет порядка 1300 о C. Здесь концентрируется расплав и заканчиваются все реакции между отдельными составляющими шихты. В этой зоне окончательно формируется металлическая фаза, штейн и шлак и происходит их разделение.
Таки образом в процессе шахтой плавки образуются три жидких продукта: черновой свинец, штейн и шлак. Состав продуктов плавки приведён в таблице 1.
Таблица 1 — Химический состав жидких продуктов плавки свинцового агломерата в шахтной печи
|
Компонент |
Продукты плавки,% |
|||
|
Свинцовый агломерат |
Черновой свинец |
Штейн |
Шлак |
|
|
Pb Cu As Sb Bi Fe S Zn SiO 2 FeO CaO MgO Al2 O2 ZnO |
5 — 36 0,5 — 1,0 10 — 15 1,0 — 2,0 5,0 — 10,0 3,0 — 5,0 7,0 — 8,0 |
92 — 98,8 0/5-7,0 0,02 — 0,3 0,1 — 0,3 0,001-0,05 0,01 — 0,1 0,1 — 0,3 0 — 0,05 |
7,5 — 29 7,0 — 37,5 7,0 — 45,0 15 — 23 5,0 — 8,5 |
|
Шлаки, содержащие значительное количество свинца и цинка подвергаются процессу возгонки в шлаковозгоночных печах (рисунок 2).
свинец черновой чугун руда
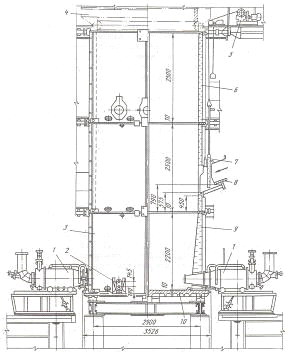
-топка — фурма; 2-летка для выпуска шлака; 3 — торцевой кессон; 4 — газоход; 5 — привод заслонки; 6 — боковой кессон; 7-заслонка; 8 — заливочное окно с жёлобом; 9-фурменный кессон; 10 — подовая плита.
Рисунок 2 Устройство шлаковозгоночной печи (фьюминговой) печи
Через загруженный в печь расплав шлака вдувают угольную пыль, служащую топливом и восстановителем. Углерод пыли сгорает до СО, который восстанавливает оксиды свинца и цинка:
ZnO + CO = Zn + CO2 + CO = Pb + CO2
В печи поддерживается температура порядка 1300о С. При этой температуре восстановленные металлы и сульфид свинца испаряются и в парообразном состоянии вытесняются на поверхность шлака. Здесь они окисляются до оксидов и и виде тонкой пыли увлекаются газами за пределы печи.
После охлаждения газов пыль улавливается в рукавных фильтрах и затем перерабатывается. Пыль содержит примерно 25% PbO и 60 — 75% ZnO. Извлечение свинца из шлака составляет 95-98%, а цинка до 90%.
Для переработки богатых свинцовых концентратов, содержащих 75-78% Pb, может быть использована горновая плавка.
Она осуществляется в горне, в который загружают практически чистый PbS, небольшое количество кокса, известь и вдувают воздух. Кислород воздуха окисляет сульфид свинца:
PbS + 3O2 = 2PbO + 2SO2
Образующийся сернистый ангидрид взаимодействует с оксидом свинца:
PbO + 2SO2 + O2 = 2PbSO4
Не окислившийся сульфид свинца взаимодействует с оксидом и сульфатом с образованием металлического свинца:
PbS + PbSO4 = 2Pb + 2SO2
PbO + PbS = 2Pb + SO2
Реакции протекают с поглощением тепла. Для компенсации тепловых потерь к шихте добавляют небольшое количество кокса.
Процесс в горне протекает при температуре 700-800о С, При этих температурах шихта остаётся в твёрдом состоянии. Капли восстановленного свинца выделяются из твердой шихты неполно. Кроме того, протекание реакции затрудняется из-за разобщения реагирующих веществ примесями. В итоге свинец извлекается неполно. Шлак содержит порядка 30% Pb и требует дополнительной переработки. Прямое извлечение в черновой свинец составляет 70%.15% свинца переходит в шлак и 15-20% в пыль. Полное извлечение свинца при переработке шлака и пыли составляет 95-97%.
В современных условиях горновая плавка может быть использована как воспомогательный процесс, позволяющий извлечь из богатых концентратов часть свинца за одну операцию при небольших затратах топлива и флюсов.
Реакционная плавка протекает по типу горновой в электрической печи. Для её осуществления необходим богатый концентрат, содержащий 65-70% Pb. Для проведения реакционной плавки свинцовый концентрат окатывают в смеси с измельчённым агломератом и пылью. Окатыши спекают на спекательной ленточной машине при температуре 800о С. Спечённые окатыши, содержащие 5-6% S, плавят в электрической печи. При температуре 1350о С. В черновой свинец и возгоны извлекается до 98% Pb. Cо шлаками теряется порядка 1,5% Pb. Выход шлака из-за малого количества флюсов невелико. Уловленные возгоны возвращаются на спекание. Главным достоинством реакционной плавки является высокий проплав и лучшие условия труда по сравнению с горновой и шахтной плавками. Недостатком плавки является то, что для её осуществления требуется богатый свинцовый концентрат.
Черновой свинец содержит 92,0 — 98% свинца. По госту содержание свинца в товарном продукте должно составлять для различных марок 99, 985-99,992%. Поэтому целью рафинирования свинца является удаление примесей до уровня стандартных норм и попутное извлечение из него благородных металлов, меди, висмута, мышьяка, олова и сурьмы. Рафинирование свинца осуществляется в чугунных или стальных котлах (рисунок 3), обогреваемых электричеством или путём сжигания углеводородного топлива.
Процесс очистки свинца от меди называется обезмеживанием. Процесс очистки основан на том, что с уменьшением температуры растворимость меди в жидком свинце уменьшается. Поэтому при охлаждении из расплавленного свинца медь выделяется. Поскольку температура плавления чистой меди (1084о С) значительно превышает температуру плавления свинца (427 о С), то медь из раствора выделяется в виде кристаллов. Поскольку медь легче, чем свинец, то кристаллы меди всплывают на поверхность расплава. Такое явление называется ликвацией. Степень очистки от меди тем выше, чем ниже температура расплава свинца.
Сначала осуществляют грубое рафинирование. Для этого расплав свинца охлаждают до 450-500о С и удаляют всплывшие кристаллы меди. Медь находится на поверхности расплава в порошкообразном состоянии и при её удалении практически не захватывается свинец. Затем расплав перекачивают в другой котёл и охлаждают до 330-340о С.
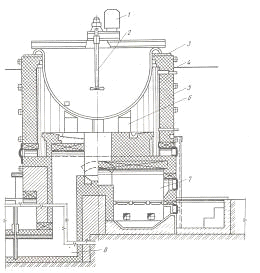
— привод мешалки; 2 — мешалка» 3-опорное кольцо; 4 — рабочая площадка; 5 — кирпичная кладка; 6 — донные опоры; 7 — топка; 8 — газоход
Рисунок 3 Котёл для рафинирования свинца
В результате образуется вязкая масса меди, пропитанная свинцом. Такие жирные съёмы направляют на первое рафинирование. Такие операции представляют собой грубое рафинирование, оно позволяет снизить содержание меди в свинце до 0,2-0,3%.
Для тонкого рафинирования в свинец с температурой 330-350о С вмешивают элементарную серу. Медь образует с ней малорастворимое в свинце соединение Сu2 S, всплывающее при отстаивании в виде твёрдых частиц. Свинец также образует с серой малорастворимый в металле сульфид PbS. Съёмы в этом случае представляют собой смесь сульфидов Cu2 S и PbS. Эти съёмы содержат до 95% Pb и 3% Cu. Они направляются вместе с жирными съёмами в первый кот1лпри обработке следующей порции чернового свинца.
Такие примеси, как олово, мышьяк и сурьма обладают большим сродством к кислороду, чем свинец. Для их удаления жидкий свинец обрабатывается жидким сплавом NaOH и NaCl, содержащим селитру NaNO3 . Селитра окисляет примеси по реакциям:
2As +2NaNO3 + 4NaOH = 2Na3 AsO4 + 2H2 O + N2
Sb +2NaNO3 + 4NaOH = 2Na3 SbO4 + 2H2 O + N2
Sn +4NaNO3 + 6NaOH = 5Na2 SnO3 + 3H2 O + 2N2
Попутно с примесями окисляется незначительное количество свинца:
2Pb +2NaNO3 + 8NaOH = 5Na2 PbO2 + 4H2 O + N2
Хлористый натрий не участвует в химической реакции, а служит только для увеличения объёма солевого расплава и понижения его вязкости.
Образующиеся в результате окисления соли примесей остаются в сплаве в виде суспензии. По мере их накопления щелочной сплав густеет, что является признаком для его удаления и расплава свинца.
Для удаления серебра и золота в расплавленный свинец при температуре 450о С добавляют цинк, который образует с серебром и золотом интерметаллические соединения Ag2 Zn2 , Ag2 Zn5 , AuZn, Au3 Zn5 , AuZn5 , которые нерастворимы в жидком свинце, более лёгкие, чем свинец и имеют температуру плавления выше, чем у свинца. Сам цинк также мало растворим в свинце, и его избыток всплывает в месте с соединениями благородных металлов, образуя на поверхности чернового свинца пену. Примеси мышьяк, сурьма и олово увеличивают расход цинка, поэтому предварительно удаляются из свинца.
Цинк вводят в жидкий свинец в несколько приёмов, путём вмешивания мешалкой. При этом снимают несколько пен. Первые из них богаты благородными металлами, последующие более бедные. Бедные пены служат оборотным продуктом. Расход цинка колеблется в пределах 1,0-1,5% от массы свинца. Богатая пена характеризуется примерным составом (%): Ag-10, Zn-25, Pb-65. Пена направляется на извлечение благородных металлов, цинка и свинца.
После обессеребрения в свинце остаётся порядка 0,7% цинка. Удаление цинка осуществляется отгонкой в вакууме. Специальными насосами жидкий свинец разбрызгивается в вакуумном пространстве. Большая поверхность капель свинца способствует быстрому испарению цинка. Пары цинка с некоторым количеством свинца в виде кристаллов конденсируются на днище стального перевернутого стакана, которое охлаждается водой. Конденсат, содержащий 60% Zn 40% Pb, используется для обессеребрения свинца.
Удаление цинка осуществляется также щелочным методом. Для этого в жидкий свинец добавляют жидкий сплав NaOH и NaCl. Цинк окисляется щёлочью по реакции:
Zn + 2NaOH = Na2 ZnO2 + H2
Полученный плав Na2 ZnO2 и NaCl выщелачивают водой для извлечения цинка и регенерации щёлочи.
Для удаления висмута в охлаждённый до 350о С свинец вводят магний и кальций, которые образуют со свинцом соединения Bi3 Ca, Bi2 Ca3 и Bi2 Mg3 . Соединения висмута с кальцием и магнием легче свинца, и имеют температуру плавления выше, чем свинец. Магний добавляют в свинец в виде чушек, а кальций — в виде 3% сплава со свинцом. Для приготовления свинцовокальциевого сплава сначала сплавляют свинец с натрием. При этом образование свинцовокальциевого сплава протекает по реакции:
[Pb-Na] + CaCl2 = [Pb-Na] + 2NaCl
Полученный сплав обрабатывают расплавленным хлоридом кальция при температуре 700о С.
Висмутовые съёмы переплавляют, отливают в аноды. В процессе электролиза висмут переходит в шлам, из которого в последующем извлекают висмут.
При совместном использовании кальция и магния удаётся снизить содержание висмута в свинце до 0,008%. Последующая небольшая добавка сурьмы позволяет снизить содержание висмута в свинце до 0,004-0,006%.
После очистки от висмута в жидком свинце остаётся избытки кальция, магния, сурьмы и небольшое количество цинка. Все эти примеси удаляют щелочным методом, окисляя их небольшим количеством селитры.
1. Лахтин Ю.М., Леонтьева В.Н. Материаловедение. Учебник для ВУЗов технич. спец. — 3-е изд. — М. Машиностроение, 2010. — 528с.
2. Материаловедение и технология конструкционных материалов. Учебник для ВУЗов / Ю.П. Солнцев, В.А. Веселов, В.П. Демьянцевич, А.В. Кузин, Д.И. Чашников. — 2-е изд., перер., доп. — М. МИСИС, 2006. — 576с.
. Материаловедение и технология металлов: Учебник для ВУЗов по машиностроительным специальностям / Г.П. Фетисов, М.Г. Карпман, В.М. Матюнин и др. — М.: Высшая школа, 2010. — 637с.: ил.
. Материаловедение. Технология конструкционных материалов: учебное пособие для студентов ВУЗов, обуч. по напр. «Электротехника, электромеханика и электротехнологии» / А.В. Шишкин и др.; под ред.В.С. Чередниченко. — 3-е изд., стер. — М.: ОМЕГА-Л, 2007. — 751с.: ил. (Высшее техническое образование).
— (Учебное пособие)
. Материаловедение: Учебник для ВУЗов, обучающих по направлению подготовки и специализации в области техники и технологии / Б.Н. Арзамасов, В.И. Макарова, Г.Г. Мухин и др. — 5-е изд., стереотип. — М.: Изд-во МГТУ им. Н.Э. Баумана, 2003. — 646с.: ил.
. Тарасов В.Л. Технология конструкционных материалов: Учеб. для ВУЗов по спец. «Технология деревообработки» / Моск. гос. ун-т леса. — М.: Изд-во Моск. гос. ун-т леса, 2006. — 326с.: ил.
. Технология конструкционных материалов. Учебник для студентов машиностроительных специальностей ВУЗов в 4 ч. Под ред.Д.М. Соколова, С.А. Васина, Г. Г Дубенского. — Тула. Изд-во ТулГУ. — 2007.
8. Технология конструкционных материалов: Учебник для студентов машиностроительных ВУЗов / А.М. Дальский, Т.М. Барсукова, Л.Н. Бухаркин и др.; Под общ. ред.А.М. Дальского. — 5-е изд., испр. — М. Машиностроение, 2003. — 511с.: ил.
