Вместе с золотом, серебром, железом, оловом, свинцом и ртутью медь входит в «великолепную семерку» металлов, известных людям с незапамятных времен. Из этих семи древнейших металлов лишь три — золото, серебро и медь — встречаются на Земле в самородном состоянии. Но золото и серебро попадались нашим предкам довольно редко, а медь значительно чаще, причем иногда в виде весьма солидных самородков [4].
Преимущества меди перед камнем в качестве материала для орудий труда, оружия, предметов быта оказались столь очевидны, что древний земледелец, скотовод или охотник не мог их не заметить. Еще бы: металл сравнительно легко менял форму, его можно было сплющить, заострить края, проделать в нем отверстие. Медь начала теснить позиции камня и вскоре прочно вошла в жизнь первобытных людей: каменный век сдал полномочия эпохе меди.
Медь и её сплавы сыграли большую роль в развитии материальной культуры. Благодаря лёгкой восстановимости оксидов и карбонатов, медь была, по-видимому, первым металлом, который человек научился восстановлять из кислородных соединений, содержащихся в рудах [6].
Цель настоящей работы, Задачи данной работы:
-
Познакомиться с химическими и физическими свойствами меди.
-
Рассмотреть свойства и значение важнейших соединений меди, а также ее сплавов с другими металлами в промышленности и жизни человека.
-
Историческая справка
Медь стала известна человеку в каменном веке – некоторые самородки меди, относящиеся к этому времени, носят следы воздействия каменных орудий, в частности у них обрублены выступающие части. Очевидно, эти кусочки меди были использованы доисторическим человеком в качестве украшений, а затем и как орудия. Распространению медных изделий способствовало свойство меди подвергаться ковке в нагретом состоянии. Так обрабатывали медные самородки индейцы еще со времен Колумба.
Где и когда был открыт метод выплавки меди из руд неизвестно. Скорее он был открыт случайно. Самородная медь всегда встречалась совместно с рудой. И вот во время нагрева самородка в раскаленных углях костра кусочки медной руды, прилипшие к самородку, тоже превратились в медь – восстановились углеродом: ![]() [3].
[3].
Добыча золота на континентах
... золота, в котором в качестве примеси содержатся медь (до 20%), палладий (от 5 до 11%), висмут (до 4%). В большинстве случаев оно содержит в виде примеси серебро ... малы, что о промышленной добыче золота не может быть и речи, так как издержки на нее были бы ... 5 г относят к самородкам. Крупнейшие из обнаруженных самородков не сохранились: переплавлены найденные в Австралии самородки «Плита Холтермана» ( ...
Руды меди часто встречаются совместно с рудами цинка, олова. Такие руды восстанавливаются легче и дают сплавы меди более твердые, чем сама медь. Эти сплавы называются бронзами, а время, в течение которого человек широко использовал бронзу, — бронзовым веком. Название “бронза” произошло от названия небольшого итальянского города Бриндизи, через который среди прочих товаров шла торговля изделиями из сплава меди с оловом. Этот сплав назвали медью из Бриндизи, а затем — бронзой.
Изготовление изделий из меди и ее сплавов производилось еще при первых фараонах Египта (4 – 5 тыс. лет до н.э.).
Известны древнейшие медные руды на острове Кипр. По-видимому, современное латинское название “купрум” произошло от латинского названия этого острова.
-
Химические и физические свойства меди
Химические свойства
а) Отношение к кислороду.
Медь проявляет к кислороду незначительную активность, но во влажном воздухе постепенно окисляется и покрывается пленкой зеленоватого цвета, состоящей из основных карбонатов меди: ![]() .
.
В сухом воздухе окисление идет очень медленно, на поверхности меди образуется тончайший слой оксида меди: ![]() .
.
Внешне медь при этом не меняется, так как оксид меди (
б) Взаимодействие с водой.
Металлы подгруппы меди стоят в конце электрохимического ряда напряжений, после иона водорода. Следовательно, эти металлы не могут вытеснять водород из воды. В то же время водород и другие металлы могут вытеснять металлы подгруппы меди из растворов их солей, например: ![]() . Эта реакция окислительно-восстановительная, так как происходит переход электронов.
. Эта реакция окислительно-восстановительная, так как происходит переход электронов.
Молекулярный водород вытесняет металлы подгруппы меди с большим трудом. Объясняется это тем, что связь между атомами водорода прочная и на ее разрыв затрачивается много энергии. Реакция же идет только с атомами водорода:![]() .
.
По химии Металлы читать бесплатно. Сообщение о металле
... большая температура плавления. Интересный факт о металлах: барий и радий обладают высокой токсичностью. Любопытно, что попавший в организм радий склонен транспортироваться более чем на 70 % в ... металлы первых четырех подгрупп. Щелочные металлы Своё название они обрели за счет свойства преобразования в щелочи в условиях водной среды. Малоизвестный интересный факт о щелочных металлах: литий обладает ...
в) Взаимодействие с кислотами.
Находясь в ряду напряжений после водорода, медь не вытесняет его из кислот. Поэтому соляная и разбавленная серная кислота на медь не действуют. Однако в присутствии кислорода медь растворяется в этих кислотах с образованием соответствующих солей: ![]() .
.
г) Качественные реакции на ионы меди.
Ион меди можно обнаружить, прилив к раствору ее соли раствор аммиака. Появление интенсивного сине-голубого окрашивания связано с образованием комплексного иона меди [ Cu ( NH 3 ) 4 ] 2+ : ![]()
Медь интенсивно окрашивает пламя в зеленый цвет.
Физические свойства
Металлы подгруппы меди, как и щелочные металлы, имеют по одному свободному электрону на один ион-атом металла. Казалось бы, эти металлы не должны особенно сильно отличатся от щелочных. Но они, в отличие от щелочных металлов, обладают довольно высокими температурами плавления. Большое различие в температурах плавления между металлами этих подгрупп объясняется тем, что между ион-атомами металлов подгруппы меди почти нет “зазоров”, и они расположены более близко. Вследствие этого количество свободных электронов в единице объема, электронная плотность, у них больше. Следовательно, и прочность химической связи у них больше. Поэтому металлы подгруппы меди плавятся и кипят при более высоких температурах [5].
а) Цвет меди и её соединений.
Чистая медь обладает следующей интересной особенностью. Красный цвет обусловлен следами растворенного в ней кислорода. Оказалось, что медь, многократно возогнанная в вакууме (при отсутствии кислорода), имеет желтоватый цвет. Медь в полированном состоянии обладает сильным блеском.
При повышении валентности понижается окраска меди, например,
б) Электропроводимость.
Медь обладает наибольшей (после серебра) электропроводимостью, чем и обусловлено её применение в электронике [2].
в) Кристаллическая решетка.
Медь кристаллизируется по типу централизованного куба (рис. 1).
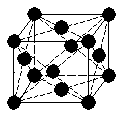

«Сварка меди и её сплавов»
... и выделяется при затвердевании в виде соединения Se 2 О. Влияние на медь аналогично влиянию серы. Классификация медных сплавов. ... восстанавливается до меди. Газы, образующиеся в результате реакций, не растворяются в твердой меди и нарушают ... сварке. Малое время существования сварочной ванны в жидком состоянии ограничивает возможности ее металлургической обработки. В частности, при раскислении меди ...
Рис. 1. Кристаллическая решетка меди
-
Важнейшие соединения меди
Медные руды — это природные минеральные образования соединений меди, содержащие ее в таких количествах, при которых промышленная добыча технически возможна и рентабельна. В первичных рудах большинства промышленных месторождений медь присутствует в сульфидной форме – CuS (сульфид меди(II)).
Приблизительно 90% известных мировых запасов меди приходится именно на сернистые руды, примерно 9% – в виде оксидных руд и менее 1% – в виде самородной меди [3].
Обычно медь в минералах находится в виде соответствующих соединений: оксиды – куприт, карбонаты – малахит, азурит, сульфаты – халькантит, брошантит, сульфиды – ковеллин, халькозин, халькопирит, борнит.
Известно около 250 минералов меди, но только 20 из них имеют промышленное значение. Главные рудные минералы меди – это халькозин или «медный блеск» Cu 2 S (79,8% меди), халькопирит или медный колчедан CuFeS 2 (30% меди), который, по оценкам, составляет около 50% всех месторождений этого элемента, борнит Cu 5 FeS 4 (52-65% меди), ковелин CuS (64,4% меди), малахит (CuOH) 2 CO 3 (57,4% меди), куприт Cu 2 O (81,8% меди).
Медь встречается в земной коре главным образом в виде комплексных соединений, содержащих, кроме меди, свинец, цинк, сурьму, мышьяк, золото и серебро.
Самые крупные месторождения в современной России находятся в Таймырском АО: Октябрьское, Талахнинское и Норильск – I, они дают две трети добычи на сегодняшний день. На одном только Октябрьском месторождении получают почти 57% российской рудничном меди [4].
По балансовым запасам меди на долю России приходится около 9% мировых, и по этому показателю мы находимся на третьем месте в мире после Чили и США. Россия в целом обеспечена разведанными запасами меди при существующем уровне добычи на 90 лет (но обеспеченность эксплуатируемых месторождений меньше, 25-30 лет).
Самые крупные в мире запасы медных руд сосредоточены в вулканических породах (порфирах) Чилийских Анд. Мировые запасы экономически рентабельных месторождений по разным оценкам составляют 340-470 миллионов тонн. При отсутствии прироста запасов и улучшения технологии добычи и производства меди современных извлекаемых запасов хватит лишь до 2050 г.
Соединения меди
Наряду с медью широкое применение в самых различных отраслях современной промышленности и сельского хозяйства находят ее соединения. Наиболее распространены соединения, в которых медь имеет степень окисления +2, реже встречаются соединения со степенью окисления меди +1. Рассмотрим некоторые соединения меди, которые наиболее часто встречаются в практической деятельности человека [6].
Коррозия меди в 5М изопропанольных растворах НС
... из меди и бронзы красивый, как говорится, «старинный» вид. А сплошной налет патины обладает еще и защитными свойствами, предохраняя ... металла. Подавляющая часть меди присутствует в горных породах в виде соединений. Из сотен минералов меди промышленное значение имеют немногие, ... ® 1/2 O 2 + H 2 O Коррозионное и электрохимическое поведение меди. В атмосферных условиях в отличие от многих других ...
Соединения меди (II):
-
Оксид меди (II) CuO
Встречается в природе и называется черной медью, мелаконитом или теноритом. Парамагнитный черный порошок (или черные кубические кристаллы).
Мало растворим в воде. Растворяется в концентрированных кислотах, при нагревании или в иодиде аммония. Растворяется в стекле, эмалях, придавая им зеленовато-синюю окраску. Применяется в производстве стекла и эмалей в качестве пигмента, в микроанализе для определения углерода, водорода и азота в органических соединениях [7].
-
Гидроксид меди (II) Cu(OH) 2
Студнеобразный синий осадок, образующийся при обработке на холоду растворов солей меди (II) щелочами. Мало растворим в воде. Проявляет слабо основные свойства. Растворяется в кислотах, аммиаке. Применяется в качестве пигмента под названием «бремовой сини».
-
Хлорид меди (II) CuCl 2
Темно-коричневые моноклинные кристаллы. Растворяется в воде, аммиаке, пиридине, эфире, спирте. Получают действием хлора на медь, взаимодействием сульфата меди (II) с серной кислотой.
-
Сульфат меди (II) CuSO 4
В безводном состоянии представляет собой белый порошок, который при поглощении воды синеет. Поэтому он применяется для обнаружения следов влаги в органических жидкостях. Водный раствор сульфата меди имеет характерный сине-голубой цвет. Из водных растворов сульфат меди кристаллизуется с пятью молекулами воды, образуя прозрачные синие кристаллы медного купороса.
Медный купорос применяется для электролитического покрытия металлов медью, для приготовления минеральных красок, а также в качестве исходного вещества при получении других соединений меди. В сельском хозяйстве разбавленный раствор медного купороса применяется для опрыскивания растений и протравливания зерна перед посевом, чтобы уничтожить споры вредных грибков [5].
Соединения меди (I):
-
Оксид меди (I) Cu 2 O
9 стр., 4129 словГазовая сварка меди, латуни, бронзы
... электродов ЗТ применяют: проволоку из меди М1, проволоку из кремнемарганцевой бронзы Бр. КМц 3–1, литые стержни из латуни Л90 или оловянно-фосфористой бронзы Бр. ОФ 4-0,25; ... свойствами. Глава I. Виды сварки меди и её сплавов. Медь сваривают ручной и автоматической дуговой сваркой, в среде защитных газов и газовой сваркой. Ручную дуговую сварку меди выполняют металлическим или угольным ...
Встречается в природе в виде минерала куприта. Диамагнитные кубические кристаллы, цвет которых меняется от коричневого до карминово-красного. Применяют в керамической промышленности в качестве пигмента.
-
Гидроксид меди (I) CuOH
Желтое соединение. Неустойчив, легко окисляется, мало растворим в воде и растворяется в аммиаке. Получают обработкой солей меди (I) щелочью при низкой температуре.
-
Сплавы меди
После того как человек научился получать и обрабатывать медь, несколько тысячелетий наряду с камнем она являлась основным твердым материалом древности. Уже первобытные металлурги пытались повысить твердость этого в чистом виде довольно мягкого металла. Первоначально, по-видимому, случайное образование сплава меди с оловом, которое могло произойти при обработке некоторых руд, содержащих вместе олово и медь, определило направление поисков улучшения механических свойств меди. Удачное соединение меди с оловом воспроизводилось человеком уже сознательно. Естественно, что испытывались композиции меди с другими металлами (цинк, мышьяк, никель и другие).
Медно-мышьяково-никелевая приколка, найденная в Азербайджане, имеет возраст более 5 тыс. лет. Предметы, изготовленные из медно-никелевых сплавов, найдены в Германии, Испании, Португалии и относятся примерно к тому же периоду.
Особое место в практической деятельности человека занимает бронза – сплав меди с оловом. Бронза превосходит медь по твердости, хорошо поддается обработке, очень устойчива к окислению. Изделия из бронзы отливались у египтян, индусов, ассирийцев. Широко использовалась бронза для изготовления украшений, статуй и других предметов художественного творчества [8].
Бронзой раньше называли только сплав меди с оловом. Теперь, помимо оловянных, широко используются алюминиевые, свинцовые, кремниевые, бериллиевые и другие бронзы.
Алюминиевые бронзы все более широко заменяют оловянные бронзы. У алюминиевых бронз литейные свойства (жидкотекучесть) ниже, чем у оловянных; коэффициент усадки больше, но они не образуют пористости, что обеспечивает получение более плотных отливок. Литейные свойства улучшаются введением в указанные бронзы небольших количеств фосфора. Бронзы в отливках используют, в частности, для котельной арматуры сравнительно простой формы, но работающей при повышенных напряжениях.
Кроме того, алюминиевые бронзы, имеют более высокие прочностные свойства, чем латуни и оловянные бронзы. Все алюминиевые бронзы, как и оловянные, хорошо устойчивы против коррозии в морской воде и во влажной тропической атмосфере. Алюминиевые бронзы используют в судостроении, авиации, и т.д. В виде лент, листов, проволоки их применяют для упругих элементов, в частности для токоведущих пружин.
Медь и цинк в организме
... как диетотерапию, так и гепатопротекторы, желчегонные средства, БАДП и препараты, содержащие цинк, бор, молибден. В случаях выраженной интоксикации применяют комплексообразователи (D-пеницилламин, купренил, металкоптаза и др.). Для понимания целебного действия меди, ... более 250 мг. 3. Индикаторы элементного статуса меди Оценку содержания меди в организме определяют по результатам исследований крови, ...
Применение кремниевых бронз, ограниченное. Используются однофазные бронзы как более пластичные. Они превосходят алюминиевые бронзы и латуни в прочности и стойкости в щелочных (в том числе сточных) средах. Эти бронзы применяют для арматуры и труб, работающих в указанных средах. Кремниевые бронзы, дополнительно легированные марганцем, в результате сильной холодной деформации приобретают повышенные прочность и упругость и в виде ленты или проволоки используются для различных упругих элементов.
Бериллиевые бронзы сочетают очень высокую прочность, коррозионную стойкость с повышенной электропроводностью. Однако эти бронзы из-за высокой стоимости бериллия используют лишь для особо ответственных в изделиях небольшого сечения в виде лент, проволоки для пружин, мембран, сильфонов и контактах в электрических машинах, аппаратах и приборах. Указанные свойства бериллиевые бронзы увеличиваются после закалки и старения, т.к. растворимость бериллия в меди уменьшается с понижением температуры [2].
Сплавы меди с цинком называют латунями (от 5 до 45%).
Латунь с содержанием от 5 до 20% цинка называется красной (томпаком), с содержанием 20–36% Zn – желтой. На практике редко используют латуни, в которых концентрация цинка превышает 45%.
Цинк более дешевый материал по сравнению с медью, поэтому его введение в сплав одновременно с повышением механических, технологических свойств, приводит к снижению стоимости — латунь дешевле меди. Электропроводность и теплопроводность латуни ниже, чем меди [4] .
Коррозионная стойкость латуней в атмосферных условиях оказывается средней между стойкостью элементов, образующих сплав, т.е. цинка и меди.
Латунь, содержащая более 20% цинка, склонна к растрескиванию при вылеживании во влажной атмосфере (особенно, если присутствуют следы аммиака).
Латуни обладают высокими технологическими свойствами и применяются в производстве различных мелких деталей, особенно там, где требуются хорошая обрабатываемость и формуемость. Из них получают хорошие отливки, так как латунь обладают хорошей текучестью и малой склонностью к ликвации. Латуни легко поддаются пластической деформации — основное их количество идет на изготовление катанных полуфабрикатов — листов, полос, лент, проволоки и разных профилей.
Латуни нашли широкое распространение и успешно используется во многих промышленных отраслях, таких, как машиностроение, приборостроение, теплотехника, производство часов, транспортных средств и санитарно-технических изделий. Кроме того, латунь используют в качестве имитатора драгоценных металлов в художественных изделиях и бижутерии, для производства духовых музыкальных инструментов, тарелок для ударных музыкальных инструментов и в производстве различных мелких деталей [3].
Марки медных сплавов.
Сплавы на основе меди
... медь - цинк (а) и механические свойства литой латуни в зависимости от содержания цинка (б) В твердом состоянии медноцинковые сплавы образуют: 1) твердый б-раствор цинка меди (типовой твердый раствор замещения) при содержании ... он ядовит, как и многие другие соединения меди, особенно для низших организмов. В малых же дозах медь совершенно необходима всему живому. Медь и ее сплавы Медь - металл ...
Марки обозначаются следующим образом. Первые буквы в марке означают: Л — латунь и Бр — бронза. Буквы, следующие за буквой Л в латуни или Бр. В бронзе, означают: А — алюминий, Б — бериллий, Ж — железо, К — кремний, Мц — марганец, Н — никель, О — олово, С — свинец, Ц — цинк, Ф. – фосфор [6].
Цифры, помещенные после буквы, указывают среднее процентное содержание элементов. Порядок расположения цифр, принятый для латуней, отличается от порядка, принятого для бронз.
В марках латуни первые две цифры (после буквы) указывают содержание основного компонента — меди. Остальные цифры, отделяемые друг от друга через тире, указывают среднее содержание легирующих элементов.
Эти цифры расположены в том же порядке, как и буквы, указывающие присутствие в сплаве того или иного элемента. Таким образом содержание цинка в наименовании марки латуни не указывается и определяется по разности. Например, Л68 означает латунь с 68% Cu (в среднем) и не имеющую других легирующих элементов, кроме цинка; его содержание составляет (по разности) 32%. ЛАЖ 60-1-1 означает латунь с 60% Cu, легированную алюминием (А) в количестве 1%, с железом (Ж) в количестве 3% и марганцем (Мц) в количестве 1%. Содержание цинка (в среднем) определяется вычетом из 100% суммы процентов содержания меди, алюминия, железа и марганца.
В марках бронзы (как и в сталях) содержание основного компонента — меди — не указывается, а определяется по разности. Цифры после букв, отделяемые друг от друга через тире, указывают среднее содержание легирующих элементов; цифры, расположенные в том же порядке, как и буквы, указывающие на легирование бронзы тем или иным компонентом [8].
Например, Бр.ОЦ10-2 означает бронзу с содержанием олова (О) ~ 4% и цинка (Ц) ~ 3%. Содержание меди определяется по разности (из 100%).
Бр.АЖНЮ-4-4 означает бронзу с 10% Al, 4% Fe и 4% Ni (и 82% Cu).
Бр. КМц3-1 означает бронзу с 3% Si и 1% Mn (и 96% Cu).
Заключение
В результате обобщения и систематизации литературных данных, посвященных меди, ее свойствам и важнейшим соединениями отмечено, что медь, ее соединения и сплавы находят широкое применение в различных отраслях промышленности [2] :
-
в электротехнике медь используется в чистом виде: в производстве кабельных изделий, шин голого и контактного проводов, электрогенераторов, телефонного и телеграфного оборудования и радиоаппаратуры;
7 стр., 3213 словМедь в организме человека
... цифры (после буквы) указывают содержание основного компонента - меди. Остальные цифры, отделяемые друг от друга через тире, указывают среднее содержание легирующих элементов. Эти цифры расположены в том же порядке, как и буквы, указывающие присутствие в ... следующим образом. Первые буквы в марке означают: Л - латунь и Бр - бронза. Буквы, следующие за буквой Л в латуни или Бр. В бронзе, означают: А - ...
-
сплавы меди с другими металлами используют в машиностроении, в автомобильной и тракторной промышленности (радиаторы, подшипники);
-
высокая вязкость и пластичность металла позволяют применять медь для изготовления разнообразных изделий с очень сложным узором. Проволока из красной меди в отожженном состоянии становится настолько мягкой и пластичной, что из нее без труда можно вить всевозможные шнуры и выгибать самые сложные элементы орнамента;
-
коэффициент линейного и объемного расширения меди при нагревании приблизительно такой же, как у горячих эмалей, в связи с чем при остывании эмаль хорошо держится на медном изделии, не трескается, не отскакивает. Благодаря этому мастера для производства эмалевых изделий предпочитают медь всем другим металлам.
Как и некоторые другие металлы, медь входит в число жизненно важных
Список литературы
[Электронный ресурс]//URL: https://drprom.ru/referat/na-temu-med/
-
Айдарова Ф.Р. Биологическая роль меди и обнаружение меди в фармацевтических препаратах / Ф.Р. Айдарова, Неелова О.В. – Успехи современного естествознания, №8, 2011. – с. 221-222.
-
Арзамасова Б.Н. Материаловедение / Б.Н. Арзамасова. Г.Г. Мухина М.: Изд-во МГТУ им. Н.Э. Баумана, 2003. – 646 с.
-
Бетехтин А.Г. Курс минералогии. Учебное пособие / А.Г. Бетехтин — М.: КДУ, 2007. — 721 с.
-
Здорик Т.Б. Минералы и горные породы / Т.Б. Здорик, Л.Г. Фельдман – М.: ABF, 1998 г. – 752 с.
-
Лидин Р.А. Химические свойства неорганических веществ / Р.А. Лидин, В.А. Молочко, Л.Л. Андреева – «Химия», 2000. – 286 с.
-
Подчайнов В.Н. Медь / В.Н. Подчайнов, Л.Н. Симонова — М.: Наука, 1990. — 279 с.
-
Угай Я.А. Общая и неорганическая химия. Учебник для вузов / Я.А Угай — М.: Высшая школа, 2002. – 304 с.
-
Фетисов Г.П Материаловедение и технология металлов / Г.П. Фетисов – М.: Высшая школа, 2009. – 624 с.
